Trong tuần này, Hội đồng Tư vấn cấp giấy phép thuốc và nguyên liệu làm thuốc của Bộ Y tế sẽ họp để xem xét cấp số đăng ký đối với thuốc chứa hoạt chất Molnupiravir cho 4 công ty dược.
Trong số này, 1 đơn vị đã có đủ nguyên liệu sản xuất trên 4,7 triệu viên thuốc chứa hoạt chất Molnupiravir.
Trước đó, có 10 đơn vị nộp hồ sơ đề nghị cấp số đăng ký cho thuốc chứa hoạt chất Molnupiravir để sản xuất trong nước. Ngoài 4 đơn vị được xem xét trong tuần này, 6 đơn vị đang bổ sung hồ sơ để xem xét cấp vào đợt sau.
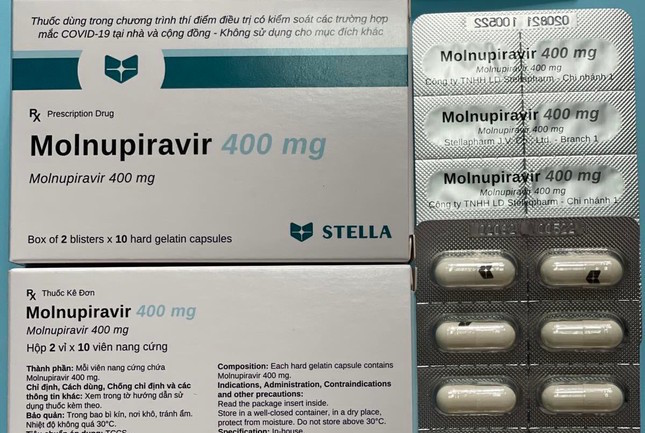
Thuốc kháng virus Molnupiravir được sử dụng cho bệnh nhân Covid-19 thể nhẹ
Bộ Y tế cho biết đến nay, một số quốc gia như Pháp, Anh, CHDCND Lào... cấp phép lưu hành cho thuốc chứa hoạt chất Molnupiravir.
Tại Việt Nam, thuốc kháng virus Molnupiravir được sử dụng tại gần 50 tỉnh thành bắt đầu từ tháng 8 vừa qua thông qua chương trình điều trị có kiểm soát do Cục Khoa học, công nghệ và đào tạo (Bộ Y tế) thực hiện.
Sau Molnupiravir, còn một số thuốc khác cũng sẽ được xem xét cấp phép theo quy định mới.
Nghị quyết giao bộ trưởng Bộ Y tế xem xét quyết định việc sử dụng dược chất đã được cấp phép nhập khẩu để sản xuất thuốc. Các thuốc mới có chỉ định điều trị Covid-19 nhập khẩu, được cấp phép có điều kiện tại một trong số cơ quan quản lý thuốc SRA (Tổ chức Y tế thế giới công bố) được cấp phép trong 10 ngày.
Các thuốc mới có chỉ định điều trị Covid-19 sản xuất trong nước nếu có cùng dạng bào chế, đường dùng, hàm lượng với thuốc đã được SRA cấp phép, Việt Nam cho phép miễn nộp hồ sơ nghiên cứu lâm sàng.
Nghị quyết này cho phép thanh toán chi phí khám, điều trị Covid-19 tại cơ sở y tế công và tư, riêng cơ sở tư nhân thanh toán theo mức phí bệnh viện đa khoa tuyến tỉnh hạng cao nhất tại địa bàn.
Theo Người lao động

















Comments powered by CComment